HDAC8是一種Zn²⁺依賴型的I類去乙酰化酶HDAC,通過催化粘連蛋白cohesin亞基SMC3去乙酰化,在細胞周期過程中發揮重要作用。HDAC8過表達能夠增強多種癌細胞的增殖、轉移及抗藥性,而其突變會導致多種嚴重的先天性遺傳疾病,例如狄朗熱綜合征(CdLS)和杜欣氏肌萎縮症(DMD)。盡管目前對HDAC8的結構和功能已有較為深入的研究,但其在細胞周期調控中的具體機製仍有待進一步闡明。
2024年7月,狗万外围充值
餘巍組在EMBO Reports在線發表題為“Reversible acetylation of HDAC8 regulates cell cycle”的文章,該研究揭示了HDAC8的可逆乙酰化修飾作為應激響應的關鍵細胞周期調節因子。
本研究發現HDAC8作為一個去乙酰化酶存在乙酰化修飾,負向調控其酶活,且HDAC8乙酰化水平在細胞周期過程中表現出動態變化。有趣的是,外部環境刺激比如葡萄糖剝奪能夠促進乙酰基轉移酶Tip60催化HDAC8乙酰化,導致粘連蛋白cohesin亞基SMC3乙酰化水平增加和細胞周期停滯。此外,構建模擬HDAC8乙酰化突變的細胞表現出廣泛的基因轉錄表達變化,這可能與三維基因組結構的改變尤其是染色質環的增強有關。數據還表明,HDAC8乙酰化通過破壞細胞周期相關基因的表達和姐妹染色單體的粘連,負向調控細胞周期進展,導致G2/M期停滯。這些發現闡明HDAC8的可逆乙酰化修飾作為一種新的細胞周期調控因子,拓展了對細胞周期動態調控過程的理解,尤其是應激響應機製。
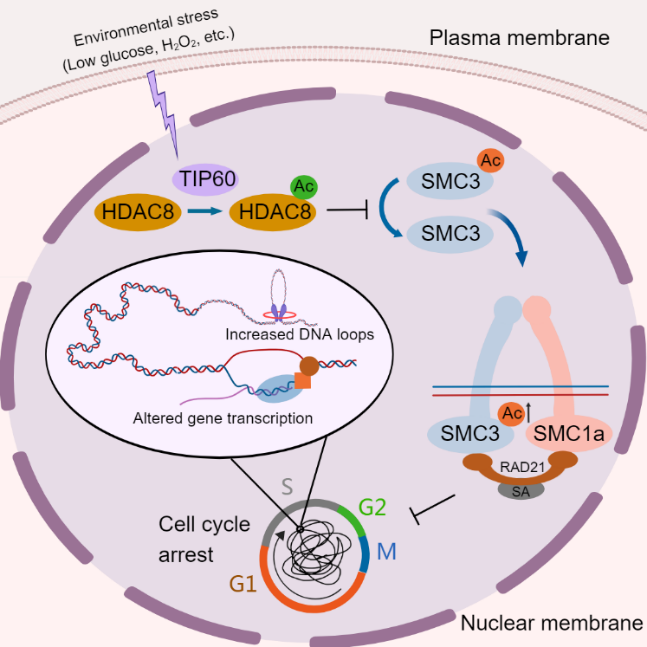
在這項研究中,課題組構建了表達模擬乙酰化突變的HDAC8-KQ 基因敲入細胞。為了研究3D基因組結構的變化,課題組對經典Hi-C技術進行了簡便而有效的改進,應用於難以大量獲取的HDAC8-KQ Knock-in細胞,顯著減少實驗過程中樣本DNA的損失。改進後的Hi-C方法能夠利用少量細胞生成高分辨率的Hi-C圖譜,這有利於拓展了Hi-C技術的應用範圍,尤其是為研究稀有臨床樣本的染色質三維結構提供了方法的支持。
HDAC8在人類病理生理學中發揮著重要功能,較為典型的是其突變可以導致罕見的多係統發育缺陷疾病——狄朗熱綜合征(CdLS)。本研究首次揭示了HDAC8在調控細胞周期過程中姐妹染色單體內聚以及染色質三維結構的重要角色,暗示CdLS患者細胞中廣泛的基因轉錄缺陷可能與HDAC8介導的染色質三維結構調控密切相關,為CdLS等HDAC8相關疾病的致病機製提供了新的見解。
本研究受到國家自然科學基金和科技部重點研發計劃資助。狗万外围充值 研究生桑超偉和李雪東為本文共同第一作者,餘巍教授是通訊作者,狗万外围充值 於淼研究員和林金鍾教授對該研究提供重要幫助。
http://doi.org/10.1038/s44319-024-00210-w

