近年來,以免疫檢查點阻斷(ICB)為代表的癌症免疫療法已經大獲成功,並成為未來治療多種腫瘤的重要基礎【1,2】。然而,腫瘤中殺傷性T細胞的係統性缺失以及複雜的腫瘤微環境均會影響免疫治療效果。因此,在臨床上急需開發出能有效促進效應T細胞在腫瘤中浸潤的新型抗腫瘤藥物。
ADP核糖基化因子1(Arf1)屬於Ras小GTPase家族成員,參與調控機體多種重要的生理過程【3-5】。然而,多項研究表明Arf1在許多人類癌症中都高表達,如肝癌、結腸癌、乳腺癌等。因此,Arf1是一個潛在的腫瘤治療靶點。然而,目前靶向Arf1的抑製劑普遍存在高毒性和特異性差的缺陷,因此,亟需開發出更加安全有效的新型Arf1抑製劑。
2023年9月6日,侯憲玉教授研究團隊在Life Metabolism雜誌上發表題為Blockade of Arf1-mediated lipid metabolism in cancers promotes tumor infiltration of cytotoxic T cells via the LPE-PPARγ-NF-κB-CCL5 pathway的研究論文。團隊前期研究發現敲除Arf1介導的脂代謝過程能有效殺死腫瘤以及癌症幹細胞(CSCs),並激發抗腫瘤免疫反應【6】。本項研究工作則重點解析了阻斷Arf1如何通過影響脂代謝從而促進細胞毒性T淋巴細胞在腫瘤內部浸潤,進而誘發抗腫瘤免疫應答的作用機製。這將為高表達Arf1的癌症患者提供一個新的治療選擇,並可能輔助現有的免疫療法改善患者臨床治療效果。

首先,團隊前期研發出的2種新型Arf1抑製劑都能顯著增加腫瘤內T細胞的浸潤程度,組織RNA測序發現趨化因子與T細胞具有強關聯性。通過檢測多種趨化因子的表達水平以及腫瘤-免疫細胞共培養係統,研究小組發現抑製Arf1主要通過上調CCL5進而影響T細胞的遷移。另外,體內實驗也表明CCL5對於Arf1缺失所介導T細胞浸潤和抗腫瘤免疫應答至關重要。
接下來為了探究抑製Arf1如何幹預CCL5轉錄的調控機製,團隊對 TCGA 數據庫中肝癌患者的 RNA 序列數據進行了相關性分析,發現與正常組織相比,過氧化物酶體增殖激活受體γ(PPARγ)信號通路在腫瘤組織中激活程度較低,說明激活PPARγ可能有助於抑製腫瘤生長。團隊發現,抑製Arf1能激活PPARγ信號通路,上調其下遊基因(CIDEC、FABP4、NR1D1和TXNIP等)的表達水平,說明PPARγ被有效激活。PPARγ 是一種轉錄調節因子【7-9】,可被不飽和脂肪酸活化。通過脂質組學分析,研究者發現,阻斷Arf1上調了多種不飽和脂肪酸(SUFA)和磷脂酰乙醇胺(PE 18:1)的水平,其中溶血磷脂酰乙醇胺 (LPE)增加最為明顯。進一步實驗結果顯示LPE確實上調了PPARγ信號通路中下遊基因的表達水平,說明抑製Arf1可能通過不飽和脂肪酸LPE影響PPARγ的激活。
有研究發現核因子kappa B(NF-κB)是CCL5的主要轉錄因子【10】。研究團隊於是進一步分析了 NF-κB是否參與CCL5 的轉錄調控。首先他們通過western blot和免疫組化(IHC)發現抑製Arf1會增加磷酸化p65的表達水平,並且ChIP-qPCR揭示NF-κB蛋白與CCL5啟動子區域的結合能力也顯著增強。而一旦阻斷NF-κB(JSH23),Arf1抑製劑通過趨化因子CCL5介導的抗腫瘤免疫效應則被明顯抑製,說明抑製Arf1可能通過NF-κB-CCL5軸招募T細胞進而發揮抗腫瘤作用。
那麼由不跑和脂肪酸LPE激活的PPARγ和NF-κB之間存在何種關聯呢?通過免疫共沉澱(Co-IP)實驗,研究小組發現LPE能削弱PPARγ和NF-κB的直接結合,而且阻斷Arf1結果亦是如此,說明Arf1能夠幹預兩者的相互作用。為了進一步探究PPARγ-NF-κB 是否會對CCL5 轉錄調控造成影響,研究團隊通過凝膠遷移實驗(EMSA)觀察到遷移條帶僅出現在CCL5探針和P65蛋白共孵育的泳道中。而當CCL5 探針與PPARγ 蛋白和 P65 蛋白一起孵育時,則沒有檢測到遷移的條帶,表明 PPARγ 蛋白和 CCL5 探針可能競爭結合P65 蛋白,充分證明了PPARγ-NF-κB-CCL5之間的作用關係。
綜上所述,阻斷 Arf1 會誘導產生不飽和脂肪酸(LPE),這種脂肪酸能結合 PPARγ 並將其從胞質PPARγ-NF-κB複合體中“奪取”出來。被“釋放”的NF-κB發生磷酸化並轉運到細胞核中,從而調節趨化因子 CCL5 的轉錄。CCL5 與細胞毒性T細胞表麵的CCR5受體結合進而招募其浸潤到腫瘤中去,最終消退腫瘤(圖1)。因此,通過阻斷Arf1調控LPE-PPARγ-NF-κB-CCL5軸能有效促進殺傷性T 細胞遷移至腫瘤內部從而發揮抗腫瘤作用,這可能為腫瘤免疫療法提供一種新策略。
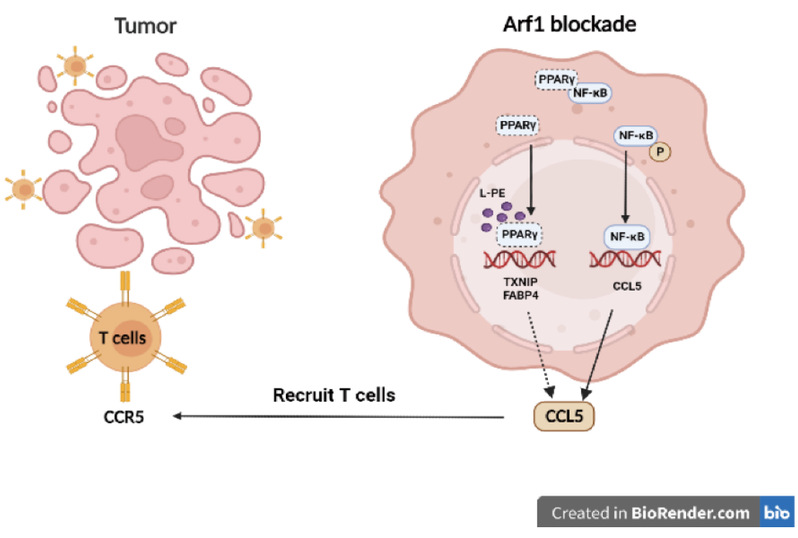
圖1. 阻斷Arf1介導的脂代謝過程進而誘發抗腫瘤免疫應答的作用機製模式圖
万博英超狼队网官方网 2019級博士研究生王娜和2021級碩士研究生姚天歌為本文的共同第一作者。狗万外围充值 生科院侯憲玉教授和王月桐青年副研究員為本文的共同通訊作者。團隊研發的新型Arf1抑製劑目前已申報了PCT國際專利。
原文鏈接:
https://doi.org/10.1093/lifemeta/load036

