2022年4月28日,我院李繼喜教授課題組在《Journal of Inflammation Research》雜誌上發表題為“Systematic Analysis of Chemokines Reveals CCL18 is a Prognostic Biomarker in Glioblastoma”研究論文,係統分析和鑒定了趨化因子在膠質母細胞瘤預後中的作用。
膠質母細胞瘤(Glioblastoma, GBM)是成人中樞神經係統中最常見的惡性腫瘤,發病率和致死率高,缺乏有效的早期診斷和治療手段,被認為是神經外科中最棘手的難治性腫瘤之一。2016年世界衛生組織(WHO)將膠質瘤分為Ⅰ至 IV級。其中GBM作為IV級膠質瘤,惡性程度最高,進展快、易複發;患者中位總生存期(Overall survival, OS)時間約為8個月,五年生存率僅為約6.8%。複雜的腫瘤微環境(TME)是導致GBM治療困難的關鍵因素之一。通過趨化因子和趨化因子受體之間的相互作用,不同的免疫細胞亞群被招募到TME中,從而實現腫瘤細胞與宿主免疫係統之間的精細調控。越來越多的研究表明,趨化因子可直接影響癌細胞增殖從而調控腫瘤進展,或通過間接調節免疫細胞的募集,影響腫瘤生長和轉移。然而,不同趨化因子對GBM預後影響的係統性分析仍然缺乏。
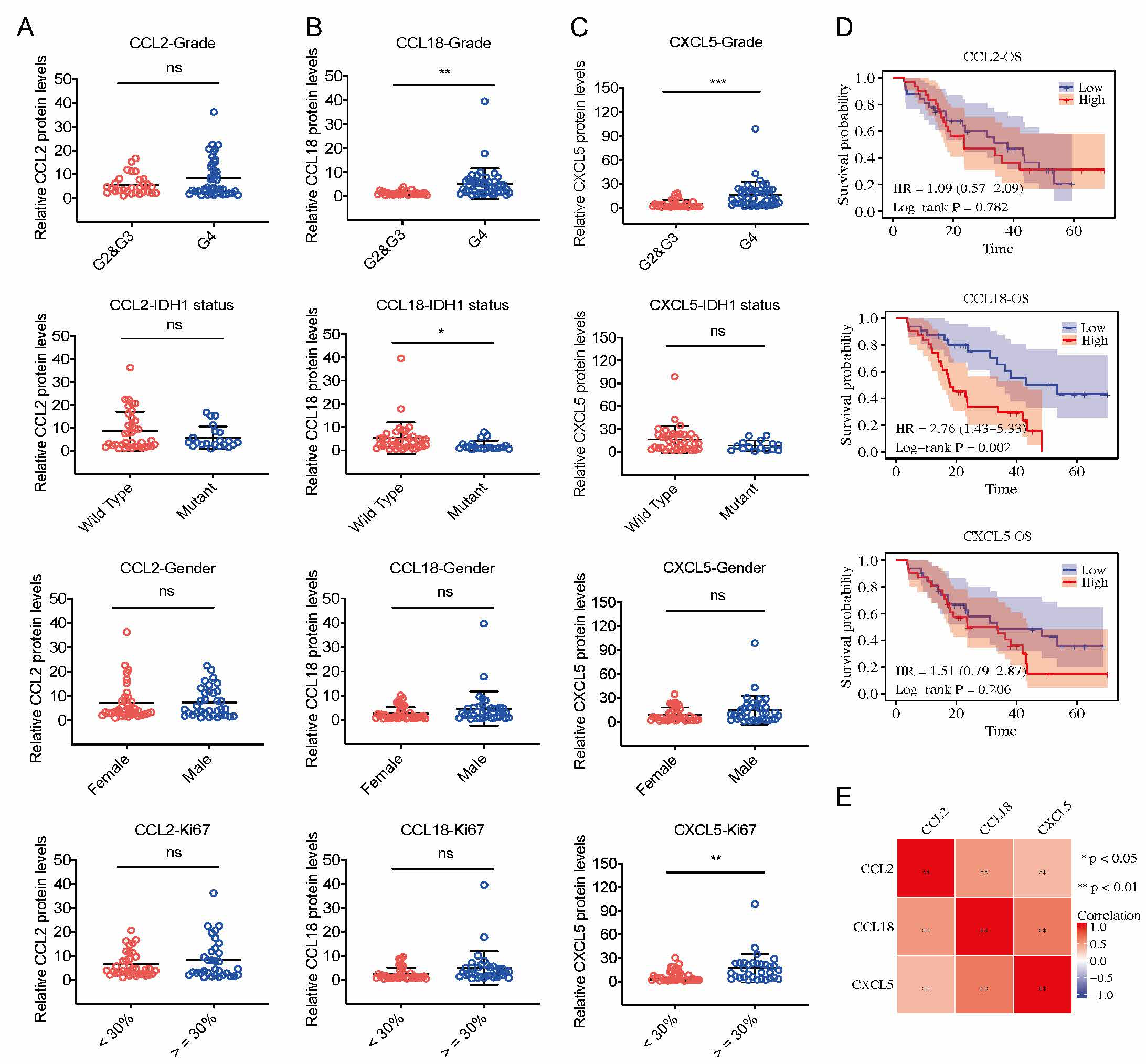
圖1,膠質母細胞瘤樣本不同趨化因子的蛋白表達水平和預後分析
万博英超狼队网官方网 李繼喜課題組長期從事細胞死亡與免疫應答研究。在本研究中,李繼喜團隊聯合溫州醫科大學蘇誌鵬團隊通過癌症基因組圖譜(TCGA) 數據庫,篩選到在膠質母細胞瘤樣本中存在差異表達的七種趨化因子基因(CCL2,CCL8,CCL18,CCL28,CXCL1,CXCL5和CXCL13)。通過Cox回歸分析,鑒定了35個趨化因子mRNA水平與膠質母細胞瘤預後的關係,其中CCL18對GBM患者具有最高的風險指數(Hazard ratio,HR),即CCL18基因高表達的GBM患者總生存期更短,提示CCL18可作為GBM診斷與預後更準確的分子標誌物。針對72份臨床膠質瘤組織樣本的檢測結果表明,CCL18在惡性程度更高的膠質瘤組織中高表達,且其高水平的蛋白表達量與患者不良預後相關。該研究對比分析了所有趨化因子在膠質母細胞瘤中發揮的作用,揭示了趨化因子CCL18在評估膠質母細胞瘤預後中的重要應用,為尋找針對膠質瘤的診斷生物標誌物和治療靶點奠定了基礎。
博士後高文青和博士研究生李媛媛為論文共同第一作者,李繼喜教授和溫州醫科大學附屬第一醫院神經外科蘇誌鵬主任為論文通訊作者。複旦附屬華山醫院神經內科陳向軍主任等給予了支持和幫助。該研究得到了國家自然科學基金及上海市科委等項目的資助。
原文鏈接:https://www.dovepress.com/getfile.php?fileID=80352

